
こんにちは くぅたろうです
技術系最高峰の国家資格【技術士】を目指している方の第一歩【技術士補】の資格
まず受かるためには過去問から勉強するのが早いです。
ただ、過去問はあるけど解説がない。解答はあるけど解説がない。
化学から技術士資格にアプローチする方の参考になればと思います。
技術士合格のための第一歩に役立てていただければ幸いです。
技術士補の化学過去問【平成29年度】
技術士補【化学】の専門科目の解答と解説を作成しました。
共通科目と適正科目は解答と解説が各サイトで載っており、また書籍でも手に入ります。
一方、過去問は技術士会のHPからダウンロードできるので誰でも見れますが、専門科目については解説が書籍でもなく、インターネットで探しても見当たりません。
ですので解答と簡単な解説を載せました。
キーワードや簡単な解説をもとに検索を広げて頂き、まずは技術士補に受かるための一歩にしていただければ幸いです。
(全ての範囲について専門的な知識があるわけではないので的確な解説ではない場合あしからず)
専門科目【化学】1

SN2反応は1段階で進行(求核剤が背面から基質の炭素に攻撃した後、脱離基が離れ始める)するが、立体障害の影響が大きく第3級ハロゲン化アルキルの場合だとほぼ進行しない。
SN2は、これが2分子反応であることを示しており、この反応は可逆的である。
よって③
専門科目【化学】2

単結合(sp3混成軌道)より二重結合(sp2混成軌道)の方が炭素間結合距離が短い。つまり炭素館結合は エタン>エチレン となる。
また、ベンゼンは二重結合で結ばれているが、共鳴しているため単結合と二重結合の中間の長さとなる。つまり ベンゼン>エチレン となる。
よって、エチレン<ベンゼン<エタン で④
専門科目【化学】3

①フェノールはクメン法で製造されるのが有名。
ベンゼンにプロペンを付加させてクメン(C6H5CH(CH3)2)を生成。空気で酸化させ、希硫酸で分解するとフェノールとアセトンが生成される。
専門科目【化学】4

A:イソプレン、B:モノテルペン、C:10個、D:黄橙色、E:視覚
よって⑤
備考:イソプレン(2-メチル-1,3-ブタジエン) / CH2=C(CH3)-CH=CH2
モノテルペン(2つのイソプレンから成る) / シトロネラール、ミルセン等
専門科目【化学】5

アセタールは塩基に対して安定
酸性条件下にて、アルコールと反応させることにより保護基が導入される。
⑤は還元的脱硫反応 (Raney-Ni)
よって②
備考:アルデヒドなどにアルコールを付加させるとアルコールとエーテルの官能基を持つヘミアセタールが生成される。
ヘミアセタールに過剰なアルコールが存在するとさらに反応し、アセタール(同一炭素原子上に2個のエーテル官能基をもつ)が生成される。
専門科目【化学】6

①正解 強力な還元剤としてカルボン酸を還元する
②正解 カルボン酸同様に水素化アルミニウムリチウムによりエステルも還元される。(水素化ホウ素ナトリウムではエステルは還元できない)
③エステルではなくカルボン酸。間違い
④正解 酸性条件では可逆反応、塩基性条件では不可逆反応。(塩基触媒で加水分解することをけん化という)
⑤正解 アミドは反応性が低く加熱することにより加水分解される。酸性条件では可逆反応、塩基性条件では不可逆反応
備考:水酸化アルミニウムリチウム(LiAlH4) や水酸化ホウ素ナトリウム (NaBH4) カルボニルの還元でよく使用される。
専門科目【化学】7
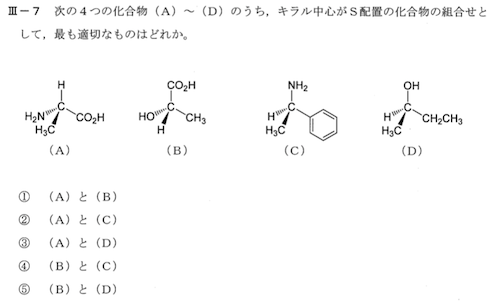
原子番号の大きいものを優先順位が高いものとし、優先順位が一番低い原子団を奥に見立て、優先順位の高いものから辿った時に反時計回りのものをS配置、時計回りのものをR配置と言う。
(A) 不斉炭素についている水素を奥に見立て、優先順位はNH2, CO2H, CH3の順となるためS配置
(B) 同様にOH, CO2H, CH3の順となるため、S配置
(C) NH2 フェニル基, CH3の順となるため、R配置
(D)OH, CH2CH3, CH3の順となるため、R配置
よって①
専門科目【化学】8

①バイオマス発電の割合は、アメリカ、中国、ドイツ、ブラジル、日本の順に高い
②正解 太陽光発電は、中国、ドイツ、日本、アメリカ、イタリアの順に高い
③正解 風力発電は、中国、アメリカ、ドイツ、インド、スペインの順(ほとんど中国)に高い
④正解 水力発電は、中国、ブラジル、アメリカ、カナダ、ロシアの順に高い
⑤正解 地熱発電は、アメリカ、フィリピン、インドネシア、メキシコ、ニュージーランドの順に高い
よって①
備考:OECD/経済協力開発機構
専門科目【化学】9

分子量が増えると分子間力が大きくなり沸点は高くなるが、枝分かれすると表面積が小さくなり分子間力も小さく成る。
共鳴安定化エネルギーによりベンゼンの総発熱量はノルマルヘキサンより低くなる。
よって⑤
備考:粘度は流体中の物体の動きにくさを表し、動粘度(=粘度/密度)は流体自体の動きにくさを表す
専門科目【化学】10

流動接触分解装置の触媒は、ゼオライト(珪酸、酸化アルミニウム)、シリカ、粘土鉱物等の物質から構成されている。
よって②
専門科目【化学】11

①正解 セタン価が高いほど自己着火しやすく、芳香族よりパラフィン系(Cが20以上のもの)の方が高い。
②煤が出ない灯芯の長さのことを煙点という。パラフィン系が多いと大きく、芳香族系が多いと小さくなる。
③正解 オクタン価は芳香族炭化水素が多く、直鎖状パラフィン系炭化水素が低い。
④正解 減圧蒸留時に生成された減圧残油を製品化したものであり、これを空気酸化させたものをブローン・アスファルトという。
⑤正解 動粘度[mm2/s]:1種20以下、2種50以下、3種(1号250以下、2号400以下、3号400以上1000以下)
よって②
備考:燃料が異常燃焼を起こす現象をノッキングという。ノッキングしにくい性質のことをアンチノック性という。
専門科目【化学】12

石油系:パラフィン系やナフテン系
非石油系:動植物油や合成潤滑油
パラフィン系は車両、工業設備油など。
ナフテン系は電気絶縁油や冷凍機油が該当する。
よって③
専門科目【化学】13

褐炭は瀝青炭より自然発火しやすいが、褐炭⇒亜瀝青炭⇒瀝青炭⇒無煙炭の順に炭素化が進んでいる。
よって⑤
専門科目【化学】14
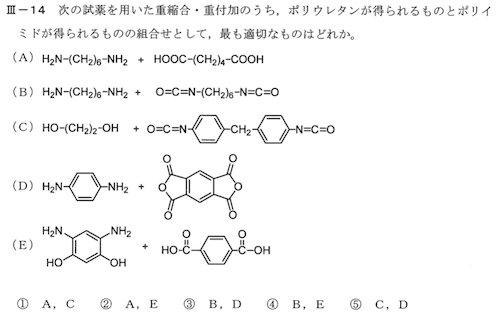
ポリウレタン(R-NH-C(=O)O-R’)はカルバメートとも呼ばれ、イソシアネートとジオールとの反応で生成される ⇒ (C)
ポリイミドはテトラカルボン酸2無水和物とジアミンとの反応 ⇒ (D)
よって⑤
専門科目【化学】15

A:ラテックス、B:塩析、C:素練り、D:加流、E:1,4ー構造
よって③
備考:イソプレンCH2=C(CH3)CH=CH2
チャールズ・グッドイヤーによって加硫法が発明される。
専門科目【化学】16

(A) ポリエステルではなくナイロン6になる。
(B) ナイロンではなくポリカプロラクトンになる。
よって①
専門科目【化学】17
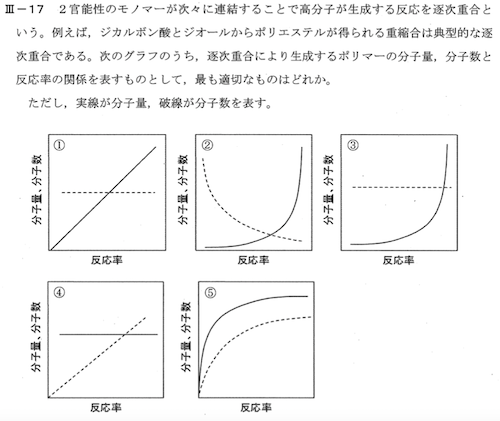
逐次重合(2つ以上の官能基モノマー間で反応する)はラジカル連鎖重合と異なり、反応率50%でも重合度はかなり低い。
反応率を99%近くまであげることにより重合度が増える ⇒ 反応率99%付近で分子量が大きくなり分子数が小さくなる。
よって②
専門科目【化学】18

ガラス転移は熱力学的な相転移(相が変わる→個体・液体・気体)と捉えられるのではなく、分子運動の凍結による速度論的転移として捉えられている。
よって④
専門科目【化学】19

5大エンプラ:ポリブチレンテレフタレート(PBT)、ナイロンPA(66)、ポリカーボネート(PC)、ポリアセタール(POM)、変性ポリフェニレンエーテル
スーパーエンプラ:ポリフェニレンスルフィド(PPS)、ポリスルホン(PSU)、ポリエーテルスルホン(PES)等
よって①
専門科目【化学】20

融解塩電解を利用して、ナトリウム、マグネシウム、アルミニウムなどが工業生産される
よって③
専門科目【化学】21

石英ガラスは実験用のビーカー・フラスコなどに使用され、急激な温度変化による影響をあまり受けない。
つまり熱膨張率は低い。
よって③
専門科目【化学】22

チタン酸バリウム (BaTiO3) は、極めて高い比誘電率からコンデンサなどの電子材料として使用されている。
よって⑤
専門科目【化学】23

地殻中の元素は酸素、ケイ素、アルミニウムの順で存在比が高い。
よって③
専門科目【化学】24

体心立方格子は周囲8個の原子と接触する。
例:ナトリウムやカリウム
よって①
備考:近接する原子数は面心立方格子(Cu, Ag, Al等)では4個、六方最密構造(Zn, Mg, Ti等)では12個
単位格子の原子数は面心立方格子では4個、六方最密構造では2個、体心立方格子では2個
専門科目【化学】25

炭酸ソーダ(炭酸ナトリウム)はソルベ法(アンモニアソーダ法)によって製造される。
NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl
NaHCO3 を熱分解すると炭酸ナトリウムが得られる。
よって①
備考:1861年エルネスト・ソルベイ
専門科目【化学】26

基底状態に戻る際に放出する光の波長は、励起準位による。
入射光のエネルギーではない。
よって③
備考:光波の位相が揃っている、重なって干渉すること(可干渉)をコヒーレントという。
専門科目【化学】27

粘度はアンドレードの式として表され、η(粘度)=B exp(E/RT)となる。(Bは比例定数)
温度上昇に伴い分子が活発になり抵抗が減る、つまり粘度が下がる。
よって①
備考:エンタルピーH = 内部エネルギーU + pV
専門科目【化学】28

仮に燃料油を100gとすると、炭素90g/12=7.5 [mol] / 水素10g/1=10 [mol]
必要な理論消費酸素は 炭素1molにつき酸素1mol, 水素1molにつき酸素10/4molより、7.5 + 2.5 = 10 [mol]
必要な理論空気量は 10 x100/21 =47.62 [mol]
実際の供給空気量は1.5倍のため 47.62 x 1.5 =71.43 [mol]
発生ガスCO2は炭素Cと同じ7.5 [mol]である。
供給された窒素量は 71.43 x 0.79 =56.42 [mol]
以上から窒素/燃焼ガス(実際の供給空気量+消費酸素+生成CO2) = 56.42 / (71.43 – 10 + 7.5) = 81.9 [%]
よって④
専門科目【化学】29

分子量1万、5万、10万のそれぞれのnNは
10/10000=0.001, 40/50000=0.0008, 50/100000=0.0005
数平均分子量は定義により、Mn=Wn/nN = (10+40+50)/(0.001+0.0008+0.0005)=100/0.0023=43,478
よって③
専門科目【化学】30

Y [g]の食塩水と仮定すると
NaCl = Y x 0.15 / 58.5 = 0.00256Y [mol] 、 H2O = Y x (1-0.15) / 18 = 0.0472Y [mol]
溶媒のモル分率は、0.0472Y/(0.0472Y + 0.00256Y) = 0.948
水の気液平衡係数KH2O = (1-0.948) / 0.1013 = 0.507
質量モル濃度は、0.00256Y/0.85Y = 0.0030 [mol/g] = 3.0 [mol/kg]
NaとClが全て解離するため3.0 x 2 = 6.0 [mol/kg]
ΔT = 0.507 x 6.0 = 3.0 [℃]
よって③
専門科目【化学】31

続きHOLD
専門科目【化学】32

気相中・液相中及び蒸気圧のベンゼン、トルエンのモル分率をそれぞれYb, Xb, pb、Yt, Xt, ptとする
ラウールの法則より
P x Yb + P x Yt = pb x Xb + pt x Xt
⇒ P(Yb + Yt) = 0.1569 x Xb + 0.0636 x (1-Xb)
Yb + Yt = 1より
P = 0.0933Xb + 0.0636
Xb = (0.1013 – 0.0636) / 0.0933 = 0.40
よって②
専門科目【化学】33

①伝熱量Q = 総括伝熱係数(U) x 伝熱面積(A) x 流体温度差平均(ΔTm)
また、②伝熱量Q = 流量 x 比熱(Cp) x 片方の温度差(ΔT) により求められる。
流体温度差平均(ΔTm) = (ΔT1+ΔT2)/2 = (150-120 + 120 – 90)/2 = 30 [℃]
①伝熱量Q = U x A x ΔTm = 540 x A x 30 = 16,200A [W]
また、②伝熱量Q = 流量(水) x Cp x ΔT = 0.5 x 4.2 x 30 = 63 [kJ/s] = 63,000 [J/s(W)]
伝熱量①②は同値のため、16200A = 63000より A= 3.89 [m2]
外径22.2[mm]から必要な伝熱管長さは 3.89/(22.2/1000 x π) = 3.89/0.07 =56 [m]
よって③
専門科目【化学】34
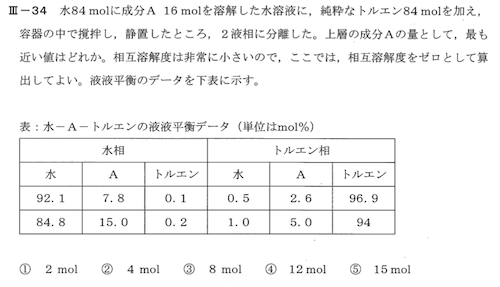
分配係数:トルエン相の成分A/水相の成分A = 2.6/7.8 = 0.33 (5.0/15 = 0.33)
トルエン相中の成分Aの濃度をXとすると、トルエン相成分A濃度/水相成分A濃度 = X/(16-X) =0.33より
⇒ X = 5.28/1.33 = 4 [mol]
よって②
専門科目【化学】35
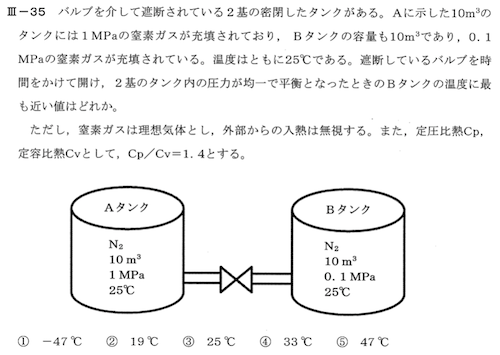
続きHOLD
技術士一次試験に合格された方は二次試験の参考にしていただければ幸いです。
[st-card id=776]
以上、最後までお読み頂きありがとうございました。









コメント